目次 Index
1. 冠動脈とPCIの基本
心臓には栄養を供給する「冠動脈」があり、右冠動脈と左冠動脈(左前下行枝と左回旋枝)から成ります。PCI(経皮的冠動脈インターベンション)は、狭くなったり詰まったりした冠動脈を拡張して血流を改善する治療です。カテーテル(直径2~3mmの細長い管)を手首、足の付け根、肘から血管に挿入し造影剤を注入してX線で冠動脈を映し出します。そして病変部にガイドワイヤーを通過させ、これをレールとして風船(バルーン)やステント(金属の網目状の筒)を持ち込み、病変部を拡張します。
2. PCIの歴史とデバイスの進化
バルーン形成術(POBA)
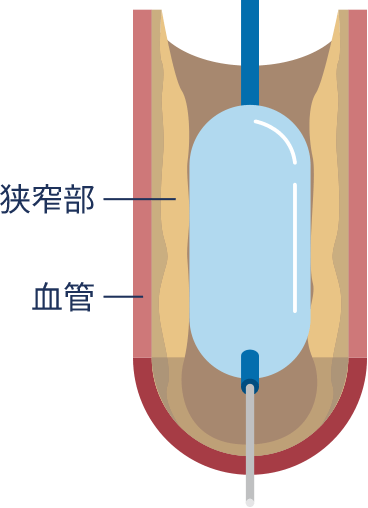
バルーン形成術(POBA)とは?
バルーン形成術は、1977年にスイスの心臓外科医アンドレアス・グルンツィヒ先生によって初めて行われました。この手術では、バルーンを使って血管を拡張し、血流を改善します。日本での初めての施術は1980年に行われ、その後、1980年代半ばには世界中の医療機関で広く採用されました。
問題点
しかし、この方法には治療後に血管が再び狭くなる「再狭窄」や、治療直後に血管が詰まる「急性閉塞」という問題がありました。
バルーン形成術(POBA)
ベアメタルステント(BMS)
金属ステントの登場
1988年に、初めて金属ステントが登場しました。このステントは血管内に設置され、血管を内側から支える役割を果たします。初期の金属ステントは薬剤が塗布されていないもので、「ベアメタルステント(BMS)」と呼ばれます。
効果と問題点
金属ステントの導入により、冠動脈の急性閉塞が大幅に減少しました。しかし、初期にはステント留置後に血栓ができる問題がありました。これを防ぐため、抗血小板薬を2種類使う治療法が有効であることがわかりました。一方、治療後に血管が再び狭くなる「ステント内再狭窄」という問題は残りました。
ベアメタルステント(BMS)
薬剤溶出性ステント(DES)
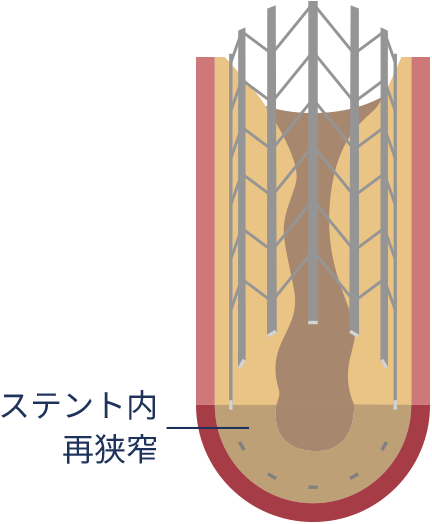
薬剤溶出性ステント(DES)の登場
2001年に、再狭窄の問題を解決するために薬剤溶出性ステント(DES)が登場しました。DESは、細胞増殖を防ぐ薬剤がコーティングされており、これが徐々に溶け出して再狭窄を防ぎます。
第1世代DESの問題
初期のDESは再狭窄を防ぐ効果がありましたが、遅発性のステント血栓症が増えるという問題がありました。これは血管の治癒反応の遅れや過剰な炎症反応が原因と考えられています。
現代のDES
その後、DESは改良され、金属の厚みが薄くなり、ポリマーの生体適合性が向上しました。これにより、遅発性ステント血栓症の問題は大幅に減少しました。現代のDESは「新世代DES」と呼ばれ、再狭窄の確率は5~10%、ステント血栓症は1%未満となり、非常に良好な成績を示しています。
薬剤溶出性ステント(DES)
生体吸収性スキャフォールド(BRS)
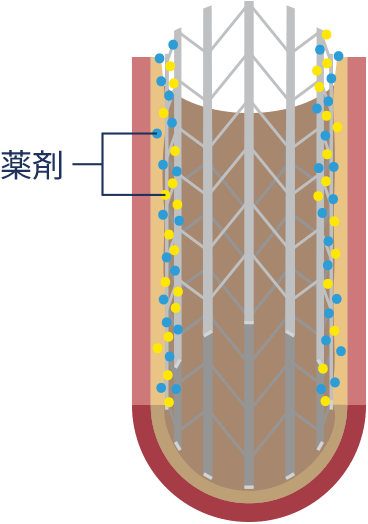
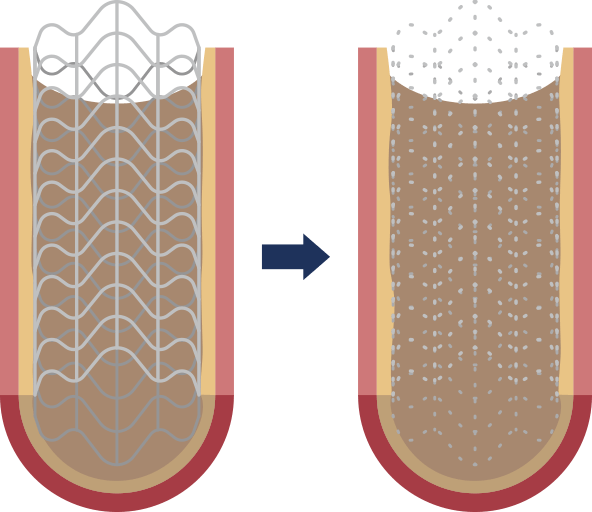
生体吸収性スキャフォールド(BRS)のコンセプト
生体吸収性スキャフォールド(BRS)は、「消えるステント」とも呼ばれ、体内に異物を残さずに血管を支える役割を果たします。役割を終えた後、数年で体内に吸収されて消失します。
歴史と課題
BRSは1998年に日本で初めて開発されました。ポリ乳酸をベースにした構造で、多くの種類が開発されましたが、最も多くの臨床試験が行われたAbsorb BVSは、新世代DESに比べ成績は劣り、また血栓症の問題もあり、2017年に製造が中止されました。
未来の期待
現在、BRSは日常診療で使用できませんが、体内に異物を残さないという魅力的なコンセプトは依然として注目されています。将来的に改良された新しいBRSの登場が期待されています。
生体吸収性スキャフォールド(BRS)
薬剤コーティッドバルーン(DCB)
薬剤コーティッドバルーン(DCB)は、バルーンに薬剤をコーティングし、それを血管壁に塗布することで再狭窄を防ぎます。
効果と適応病変
2006年に、ステント内再狭窄病変に対するDCBの効果が報告されました。その後、様々な臨床試験が行われ、新しい冠動脈病変にも有効であることがわかりました。2014年から日本でも使用が開始され、現在2種類のDCBが利用可能です。
メリットと使用上の制約
DCBはステントを留置せずに治療を完了できるため、体内に異物を残さないという長期的なメリットがあります。使用頻度は年々増加していますが、バルーン拡張の際に血管に大きな傷を残さないことが重要です。
薬剤コーティッドバルーン
(DCB)

3. PCIの適応
PCIの対象となる虚血性心疾患
虚血性心疾患とは?
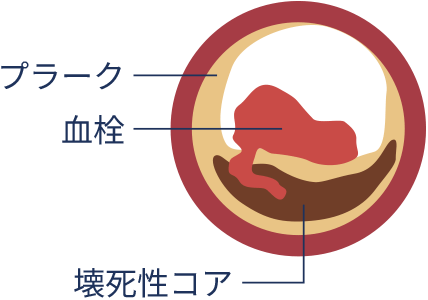
PCIの対象となる虚血性心疾患(冠動脈疾患)は、主に動脈硬化が原因で発生します。動脈硬化は、冠動脈内に脂質や石灰がたまって血管が狭くなることで進行します。進行した脂質沈着は「壊死性コア」と呼ばれ、これを覆う被膜が破裂すると血栓が形成され急性閉塞を引き起こすことがあります。
慢性冠症候群とは?
冠動脈に血栓がない場合は「慢性冠症候群(安定冠動脈疾患)」と呼ばれ、動いた時に胸痛が現れる「労作性狭心症」や、症状がない「無症候性心筋虚血」が含まれます。
慢性冠症候群(安定冠動脈疾患)

- 労作性狭心症
- 無症候性心筋虚血
急性冠症候群とは?
急性冠症候群は血栓が形成された状態です。これには完全に血管が詰まる「ST上昇型急性心筋梗塞」と、完全には詰まらない「不安定狭心症」や「非ST上昇型急性心筋梗塞」が含まれます。
症状と危険性
急性心筋梗塞は、突然の血流障害で心筋細胞が壊れる病気で、突然死の原因になることもあります。
急性冠症候群
- 不安定狭心症
- 急性心筋梗塞
(非ST上昇型)

- 急性心筋梗塞
(ST上昇型)
急性冠症候群へのPCI
急性冠症候群に対するPCIの重要性
急性冠症候群に対するPCIは、死亡率を減少させる効果的な治療法として広く受け入れられています。特に発症12時間以内の急性心筋梗塞に対する再灌流療法の有効性が確立されています。
治療の目標
急性心筋梗塞では、患者が病院に到着してから90分以内に冠動脈の血流を再開させること(door-to balloon time90分以内)が目標です。
再灌流の方法
再灌流の方法には、PCIのほかに血栓溶解療法(注射で血栓を溶かす治療)や冠動脈バイパス術(CABG)があります。PCIは血栓溶解療法に比べて効果が高く、現在は標準的な治療法とされています。血栓溶解療法を行わずに緊急で行うPCIは「プライマリーPCI」と呼ばれます。
急性心筋梗塞症例へのPCI施行時の冠動脈造影画像
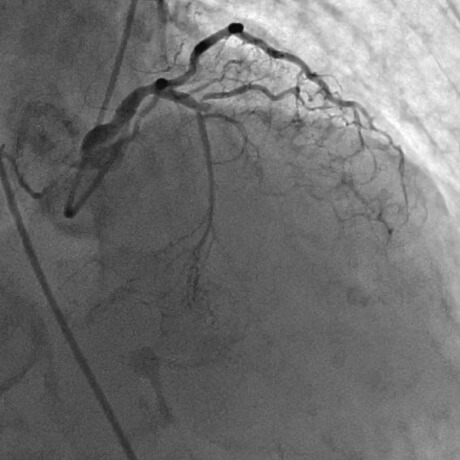
冠動脈が完全閉塞した急性心筋梗塞
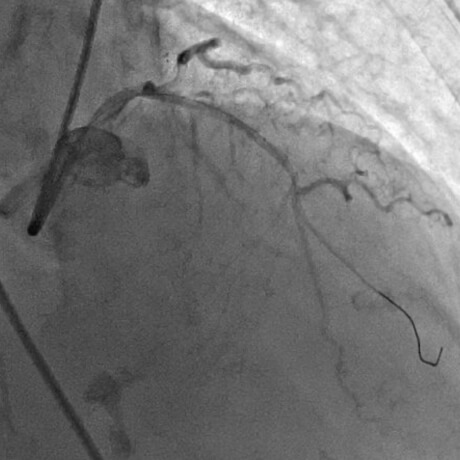
ワイヤーの通過でわずかに血流改善
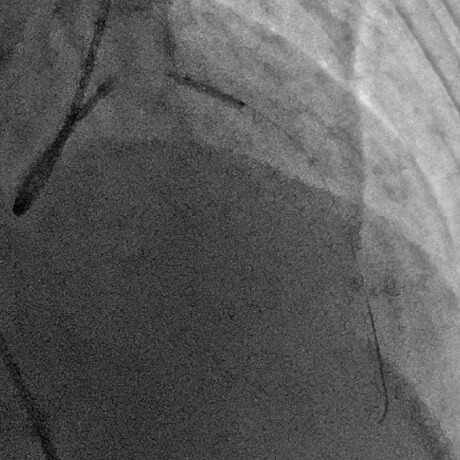
バルーンで閉塞部を拡張
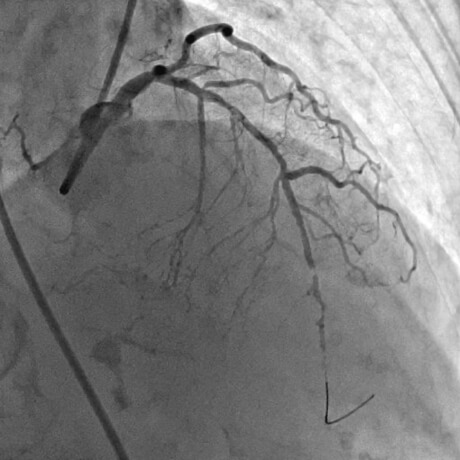
血流は良好に改善したが、拡張は不十分
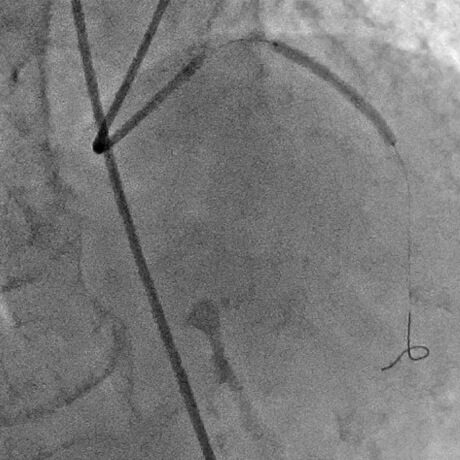
薬剤溶出性ステントを拡張中
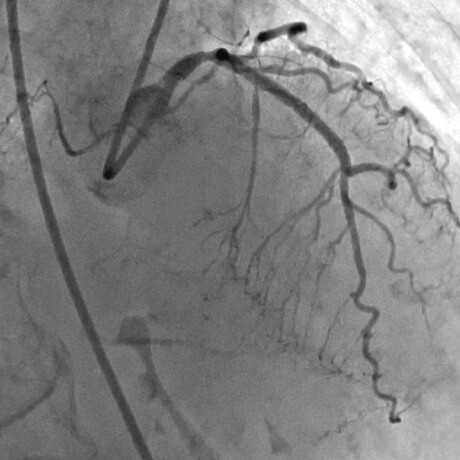
治療後最終の造影
慢性冠症候群へのPCI
慢性冠症候群へのPCIの効果
慢性冠症候群に対するPCIの生命予後改善効果は確立されていません。しかし、胸痛の症状改善や生活の質(QOL)の向上に効果があります。
将来のリスク低減
PCIは手技関連の心筋梗塞リスクを増加させますが、将来的な自然発症の心筋梗塞を減少させることができます。
薬物治療との併用
現在は薬物治療も進歩しており、十分な薬物治療を行った上で冠動脈造影やPCIを検討することが一般的です。
重症冠動脈病変の評価
重症冠動脈病変の場合、薬物治療のみでは効果が不十分であることが多く、PCIやCABGによる血行再建が検討されます。したがって重症冠動脈病変か否かの評価は早めに行うことが望ましく、その方法として非侵襲的な冠動脈CTがよく行われます。
PCIの慎重な適応
PCIは侵襲的な処置であり、合併症のリスクがあるため、特に慢性冠症候群に対しては慎重な適応が求められます。現在の適応条件は以下の通りです。
適応条件
- 冠動脈造影で90%以上の狭窄がある場合
- 狭心症の原因と考えられる狭窄がある場合
- 機能的虚血の評価で原因が狭窄と確認された場合
虚血の評価
「虚血」とは心筋の血流が不足している状態を指します。見た目の狭窄度だけでなく、以下のような方法で評価することができます。
- 核医学検査(心筋シンチグラフィー)
- 運動/薬剤負荷心エコー
- 運動負荷心電図
- 心筋血流予備量比(FFR)
FFRとは?
FFR(Fractional Flow Reserve)は、冠動脈内の血流の圧力差を測定することで虚血を評価する方法です。薬剤を使って冠動脈を最大限に拡張させ、病変の前後の圧力を比較します。FFR値が0.80以下の場合、虚血があると判断されます。
安静時指標とは?
安静時指標は、FFRと同様に圧センサー付きのガイドワイヤーを使用しますが、冠動脈を拡張させる薬剤を使いません。以下のような指標があります。
- iFR(Instantaneous wave-free ratio)
- dPR(Diastolic pressure ratio)
- RFR(Resting full-cycle ratio)
- DFR(Diastolic hyperemia-free ratio)
これらの方法で0.89以下の値が出た場合、虚血があると判断されます。
心筋血流予備量比
FFR(fractional flow reserve)
= PdPa (0.80以下で虚血陽性)
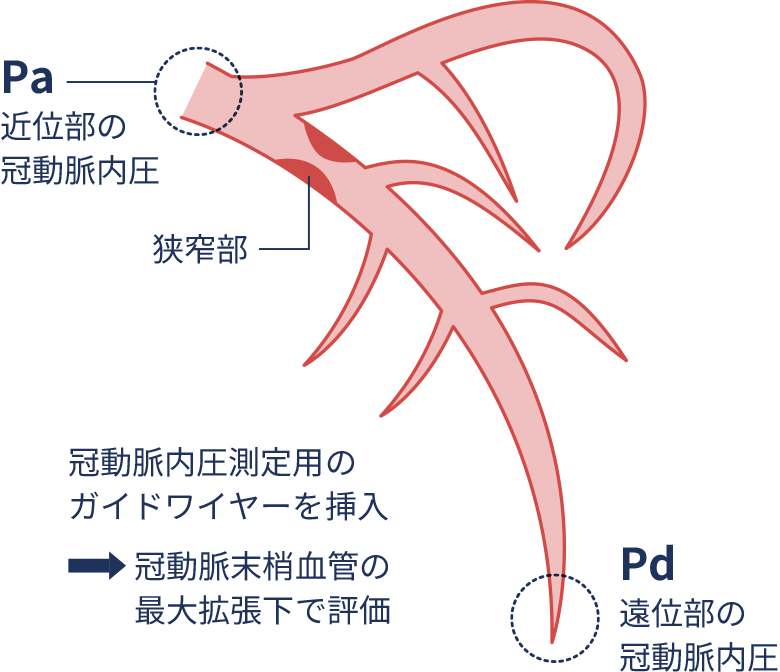
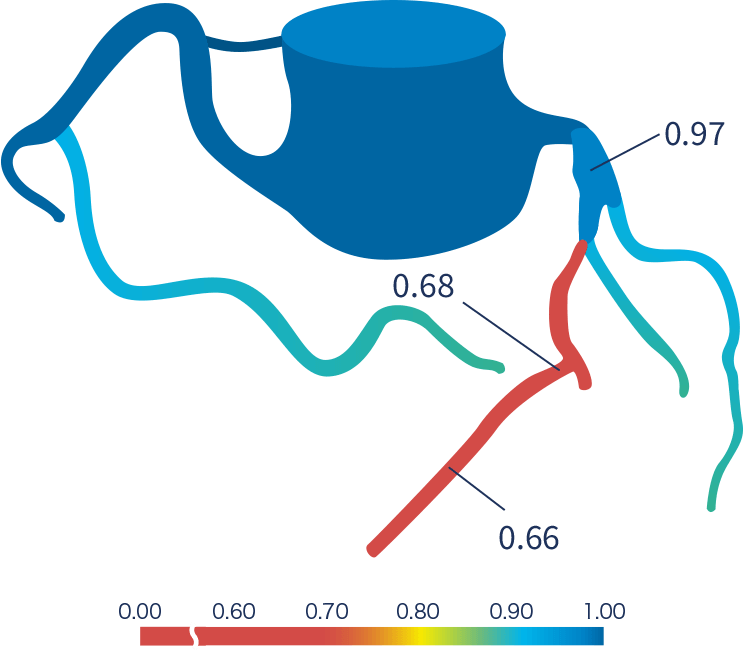
FFR-CTとは?
最近では、圧センサー付きのガイドワイヤーを使わずに、冠動脈CTの画像データをスーパーコンピューターで解析して、非侵襲的にFFR値を算出する方法(FFR-CT)が普及しています。
FFR-CT
PCIの合併症
PCIの負担とリスク
PCIは外科手術に比べて体への負担は少ないですが、侵襲的な処置であり、いくつかの合併症のリスクがあります。
考えうる合併症
- 血管損傷(穿刺部や冠動脈など)
- 血栓塞栓症(脳梗塞など)
- 出血(穿刺部、消化管など)
- 腎機能障害(造影剤の使用による)
- アレルギーや感染症
- 放射線被ばく関連の合併症(皮膚炎など)
冠動脈への処置によるリスク
- 末梢塞栓(血栓やプラークが冠動脈末梢を閉塞)
- 側枝閉塞(太い冠動脈を拡張した際の枝の閉塞)
- 冠動脈解離・穿孔(冠動脈壁の裂けや穴)
これらの合併症により、急性心筋梗塞を併発することや緊急手術が必要になることもあります。
適応の評価と意思決定
PCIは上記のような合併症リスクを伴う処置であるため、治療による利益とリスクを十分に考慮し、医療従事者と患者さん・ご家族がよく話し合って意思決定を行うことが重要です。
PCIとCABGの治療選択
冠動脈の血行再建法
冠動脈の血行再建には、PCIのほかにバイパス手術(CABG)があります。CABGは、体内の他の血管を冠動脈の病変部の遠位に接続する手術です。全身麻酔下で行われ、胸部を開くことが一般的ですが、場合によっては小さな切開のみで行われることもあります。
治療法の選択
PCIとCABGのどちらが良いかは、以下の要素を考慮します。
- 冠動脈病変が1枝か多枝か
- 冠動脈病変の複雑さ
- 糖尿病の有無
- 左主幹部の病変の有無
治療の決定
治療方針は、ガイドラインに基づき、患者さんの臨床背景や意向を考慮して決定されます。一人の医師の意見のみではなく、循環器内科医や心臓外科医を含むチームでの議論を経て、最善と考えられる治療法の提案が成された上で、最終的な患者さんの意思決定に基づいて治療方針が決定されることが重要です。
4. PCI手技の実際
PCIの手術環境
PCIは局所麻酔薬を使用して行われるため、通常は覚醒した状態での処置となります。専用のX線装置がある治療室で行われ、患者さんは仰向けになります。
手技の実施
術者は患者さんの右側に立ち、医師の助手、看護師、臨床工学技士、放射線技師などが協力して手技をサポートします。患者さんのケアや医療機器の操作、X線装置の調整を行いながら手技を進めます。
治療の流れ
カテーテル挿入手順
-
消毒と麻酔
カテーテルを挿入する部位(手首、大腿、肘など)を消毒し、局所麻酔を行います。
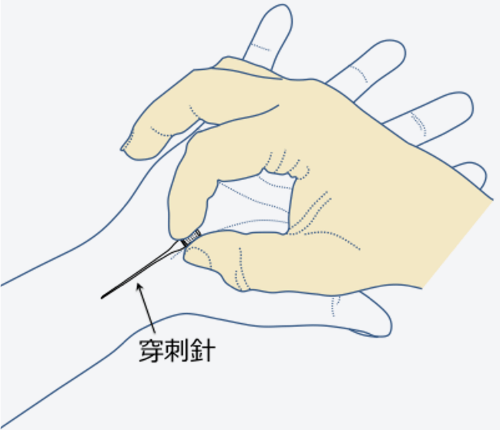
-
穿刺
針で動脈に穴を開け、ワイヤーを挿入します。
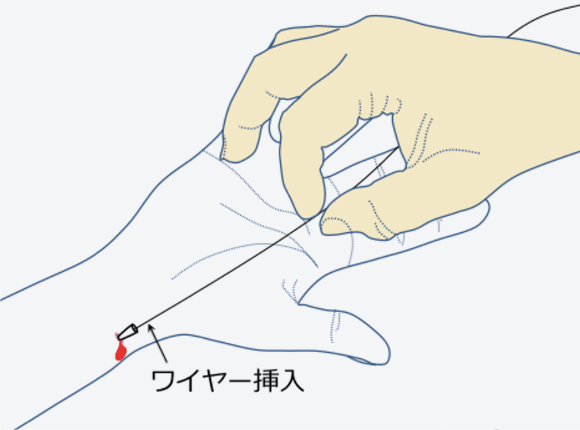
-
シースの挿入
ワイヤーを通してシースを挿入し、カテーテルの出し入れを安全にします。
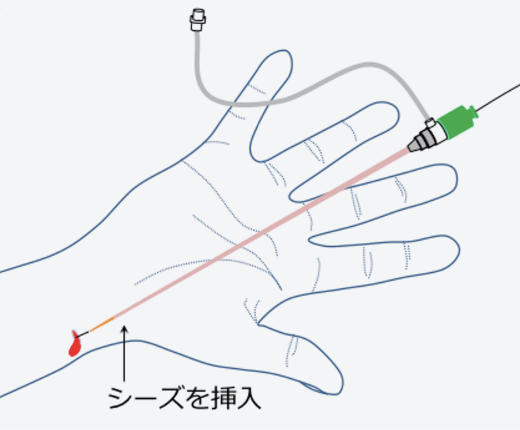
-
抗凝固薬の
投与血栓を防ぐために抗凝固薬を投与します。
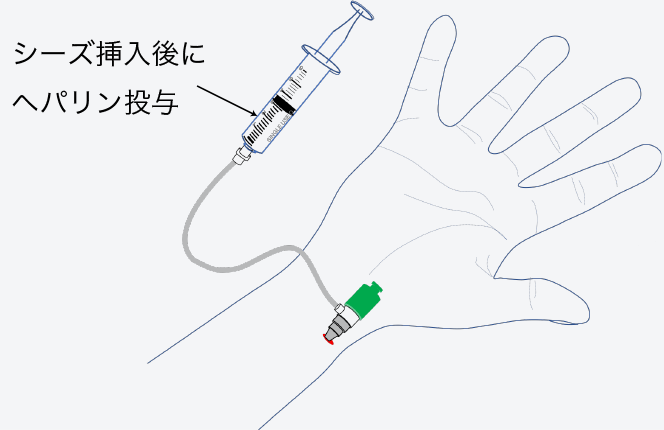
-
ガイディング
カテーテルの挿入シースを通してガイディングカテーテルを冠動脈の入口まで進めます。
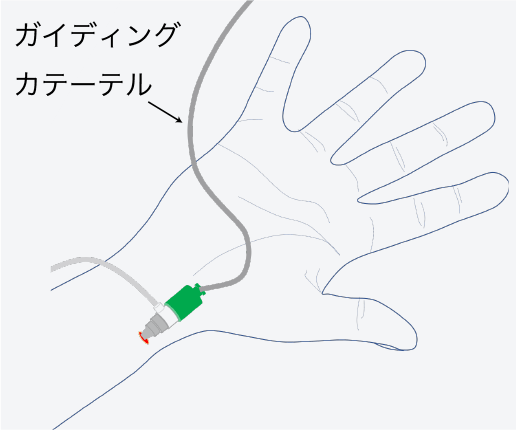
-
造影と評価
造影剤を注入し、X線で冠動脈の狭窄や閉塞部位を評価します。
-
ガイドワイヤー
の挿入ガイドワイヤーをカテーテルに通して冠動脈内に挿入し、狭窄部や閉塞部を通過させます(図a,b)。ガイドワイヤーは、バルーンカテーテルなどの機器が冠動脈内を走行するためのレールの役割をします(図c)。
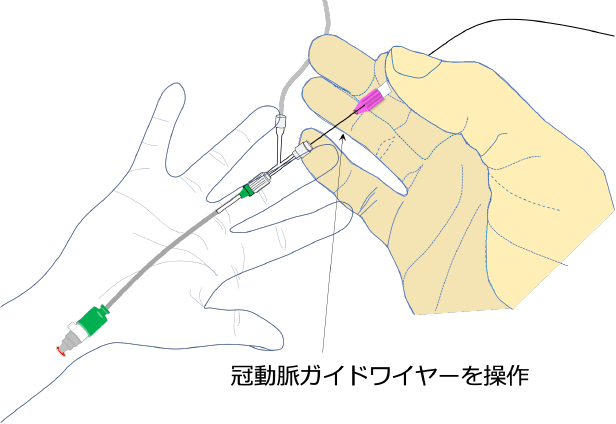 図a
図a
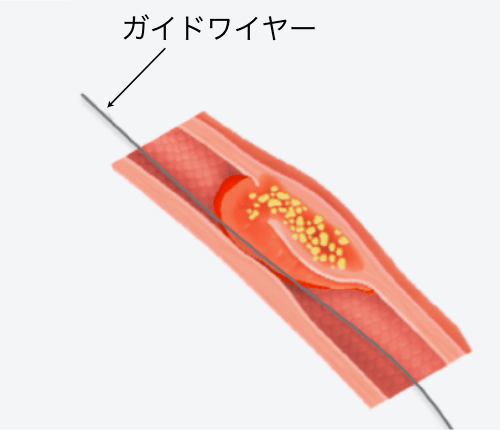 図b
図b
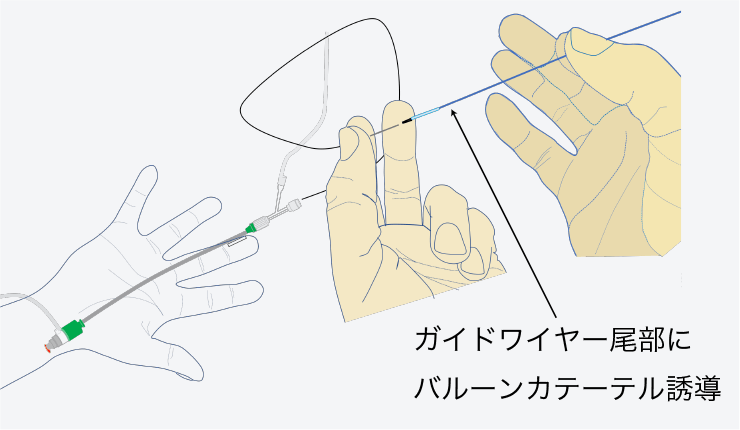 図c
図c
-
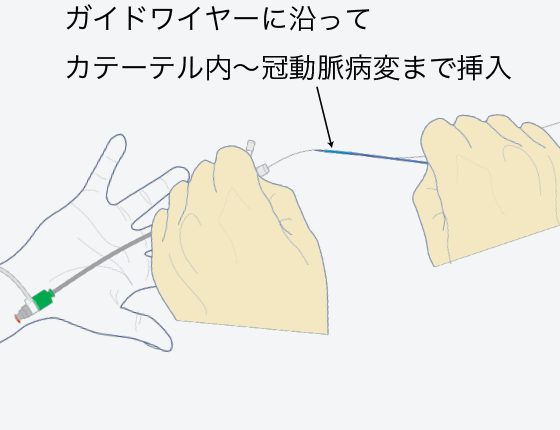
バルーン
カテーテル挿入バルーンカテーテルの先端をガイドワイヤーに沿わせて冠動脈内に進めます。
-
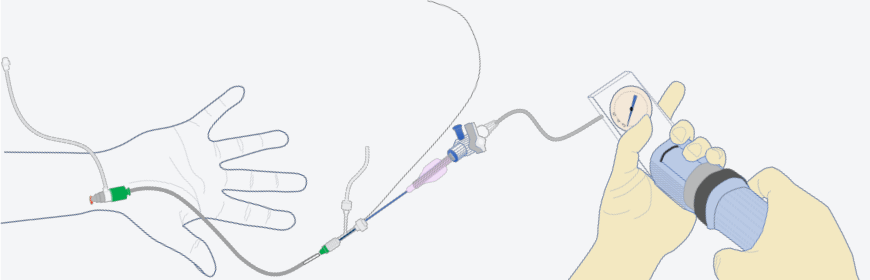
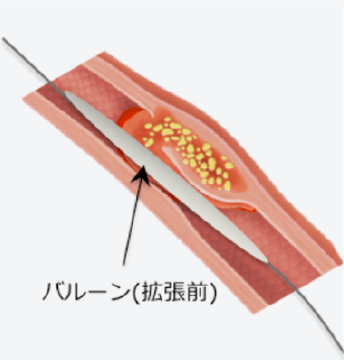
バルーン拡張
バルーンを病変部まで進めた後、拡張機器を接続し、圧を加えてバルーンを拡張します。
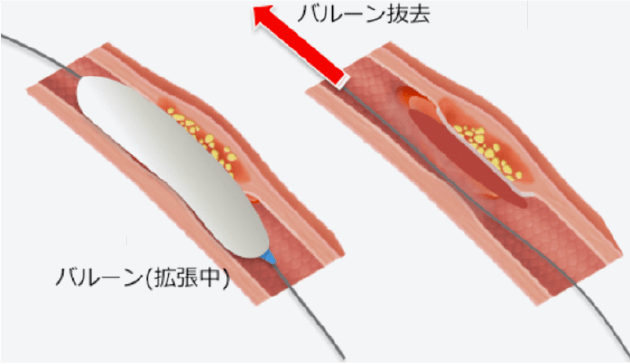
-
ステントの設置
多くのPCIでは、バルーンでの拡張後に冠動脈ステントを留置します。ステントはバルーンの外側に折りたたまれており、バルーンを拡張することで冠動脈内に展開されます。
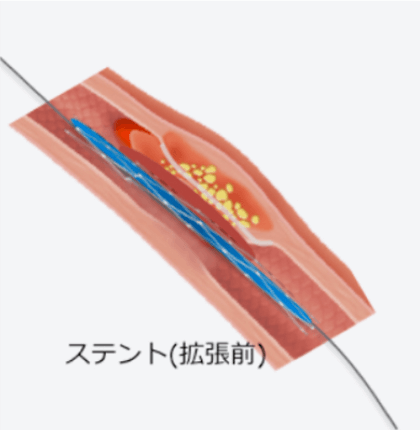
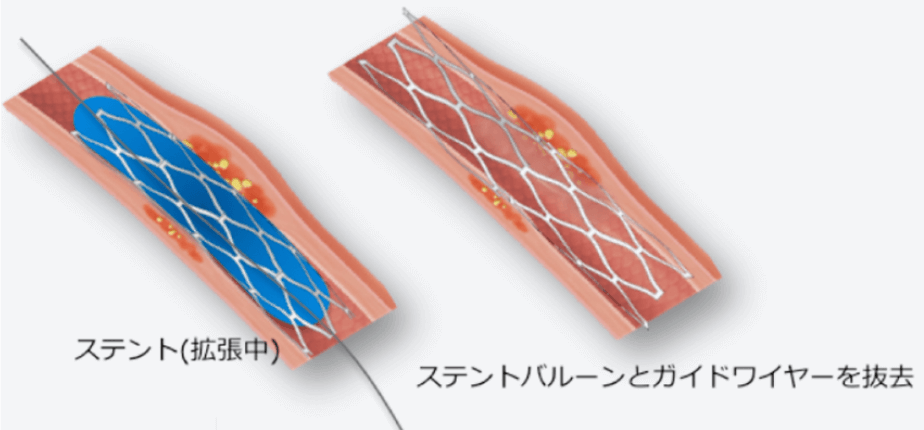
-
手技の終了
手技終了時にはバルーンカテーテル、ガイドワイヤー、ガイディングカテーテルを体外に回収しますが、ステントは冠動脈内に残ります。
血管内画像診断装置の併用
日本のPCIでは、血管内超音波(IVUS)や光干渉断層法(OCT/OFDI)と呼ばれる血管内画像診断装置がよく使われます。ガイドワイヤーに沿わせてこれらの機器を冠動脈内に挿入し、超音波や近赤外線による画像診断で冠動脈の断面像を取得します。これにより、バルーンやステントのサイズを適切に決定できます。
特殊デバイスの併用
PCIでは、バルーンやステント以外に特殊デバイスが使用される場合があります。
冠動脈アテレクトミー
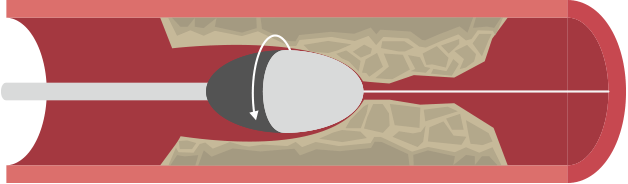
冠動脈の石灰化が高度な場合、ドリルのようなもので石灰化を削る「冠動脈アテレクトミー(ローテーショナルアテレクトミー/オービタルアテレクトミー)」が使用されます。
ローテーショナルアテレクトミー
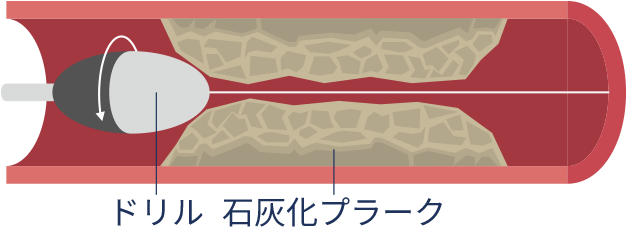

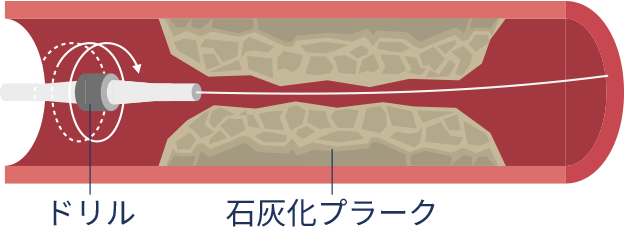
オービタルアテレクトミー
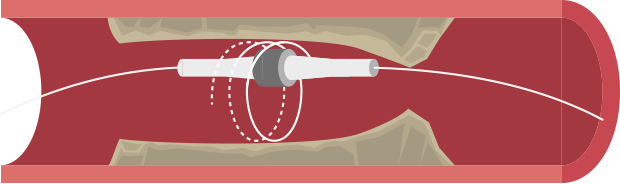

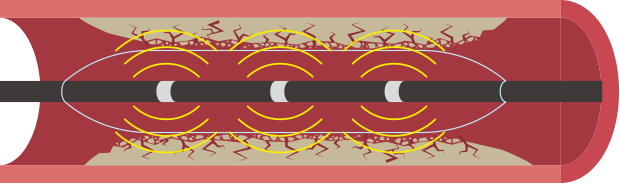
IVLデバイス
高速音圧波で石灰化を破砕する「Intravascular lithotripsy(IVL)」というデバイスも使用されることがあります。
IVL


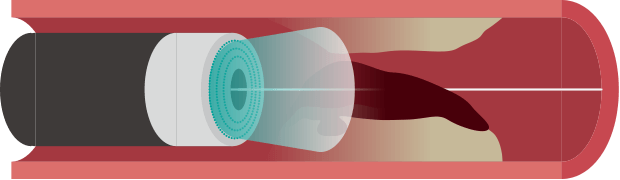
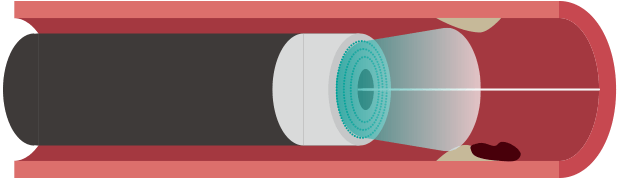
方向性粥腫切除術(DCA)
左冠動脈主幹部や左前下行枝入口部の病変では、プラークを直接削るデバイスを使用する「方向性粥腫切除術(DCA)」が行われることがあります。これにより、ステントの使用を回避したり、バルーン拡張後の側枝閉塞を防いだりできます。
方向性粥腫切除術(DCA)
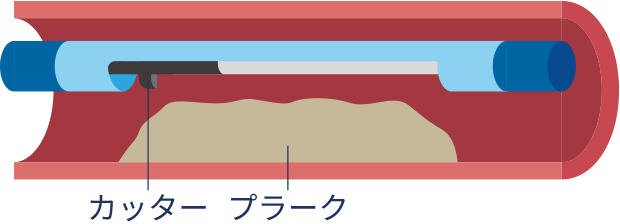
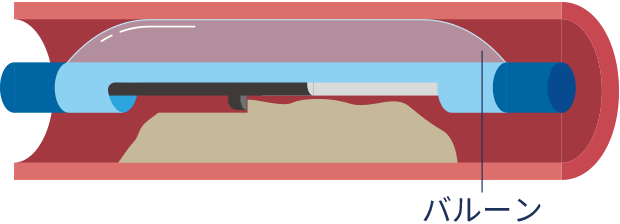
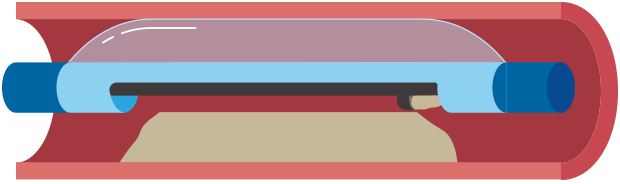
エキシマレーザー冠動脈形成術(ELCA)
多量の血栓やステント内再狭窄の場合、レーザーで血栓やプラークを蒸散させる「エキシマレーザー冠動脈形成術(ELCA)」が併用されることもあります。
エキシマレーザー(ELCA)
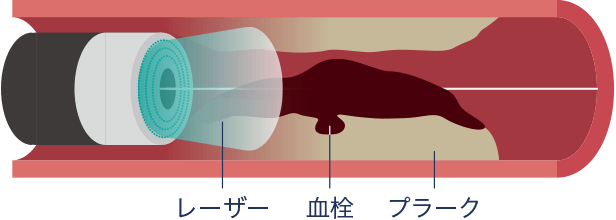
これらの特殊デバイスは、すべての施設で使用できるわけではありません。使用可能な施設は、基準を満たしているか、必要な機器が配備されている施設に限られます。この手技は専門医が適切な施設で行うことが重要です。
手技終了後の処置
シースの抜去と止血
手技終了後、動脈に挿入されたシースを抜去し、穿刺部の止血を行います。
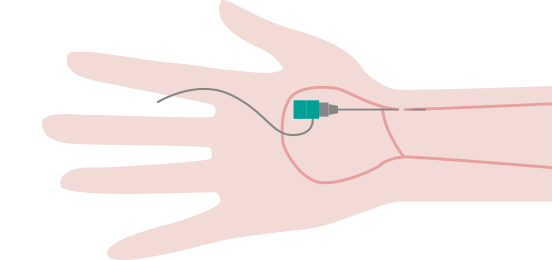
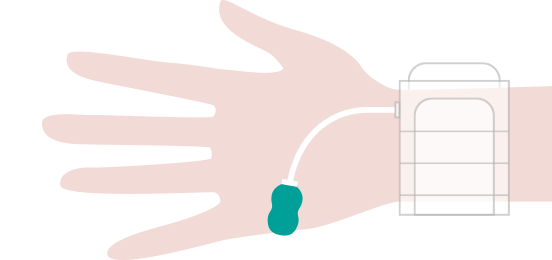
橈骨動脈の止血
手首の穿刺の場合、リストバンドのような器具で圧迫止血を行います。これにより、手技終了後すぐに歩行可能です。
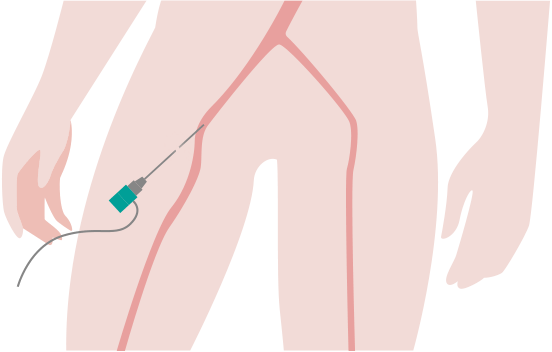
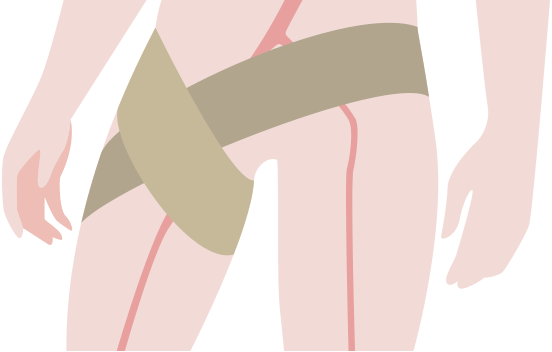
大腿動脈の止血
足の付け根の穿刺の場合、シース抜去後は数時間の安静が必要です。ただし、止血デバイスを併用することで安静時間が短縮されることもあります。
退院までの期間について
待機的PCIの場合
慢性冠症候群に対する待機的PCIでは、大きな合併症がなければ、術後1~2日で退院が可能です。
急性冠症候群の場合
急性冠症候群の場合、心臓が受けたダメージの程度によりますが、術後の心臓リハビリテーションが非常に重要なため、数日から数週間の入院が一般的です。
5. PCI後の薬物治療
薬物治療の重要性
PCIやCABGを行った後も、薬物治療は重要です。特に虚血性心疾患の発症や再発を予防するためには、薬物治療が柱となります。
治療の目的
PCI後の薬物治療は、以下の2点を主な目的とした治療です。
- 抗血栓療法
血栓を防ぐための治療 - 動脈硬化の進展予防
動脈硬化の進行を防ぐための治療
心筋梗塞後の治療
心筋梗塞後の患者さんでは、これらに加えて心不全の発症や進行を予防する薬物治療も必要です。
抗血栓療法
抗血小板薬2剤併用療法(DAPT)
PCI後は、冠動脈内の血栓を防ぐために、一定期間抗血小板薬を2種類併用するDAPTが必要です。特に薬剤溶出性ステント(DES)の使用後は重要です。
DAPT期間の短縮化
長期間のDAPTは出血のリスクがあるため、短期間のDAPTが推奨されるようになっています。日本循環器学会のガイドラインでは、出血リスクに応じたDAPTの期間が示されています。
ガイドラインの推奨
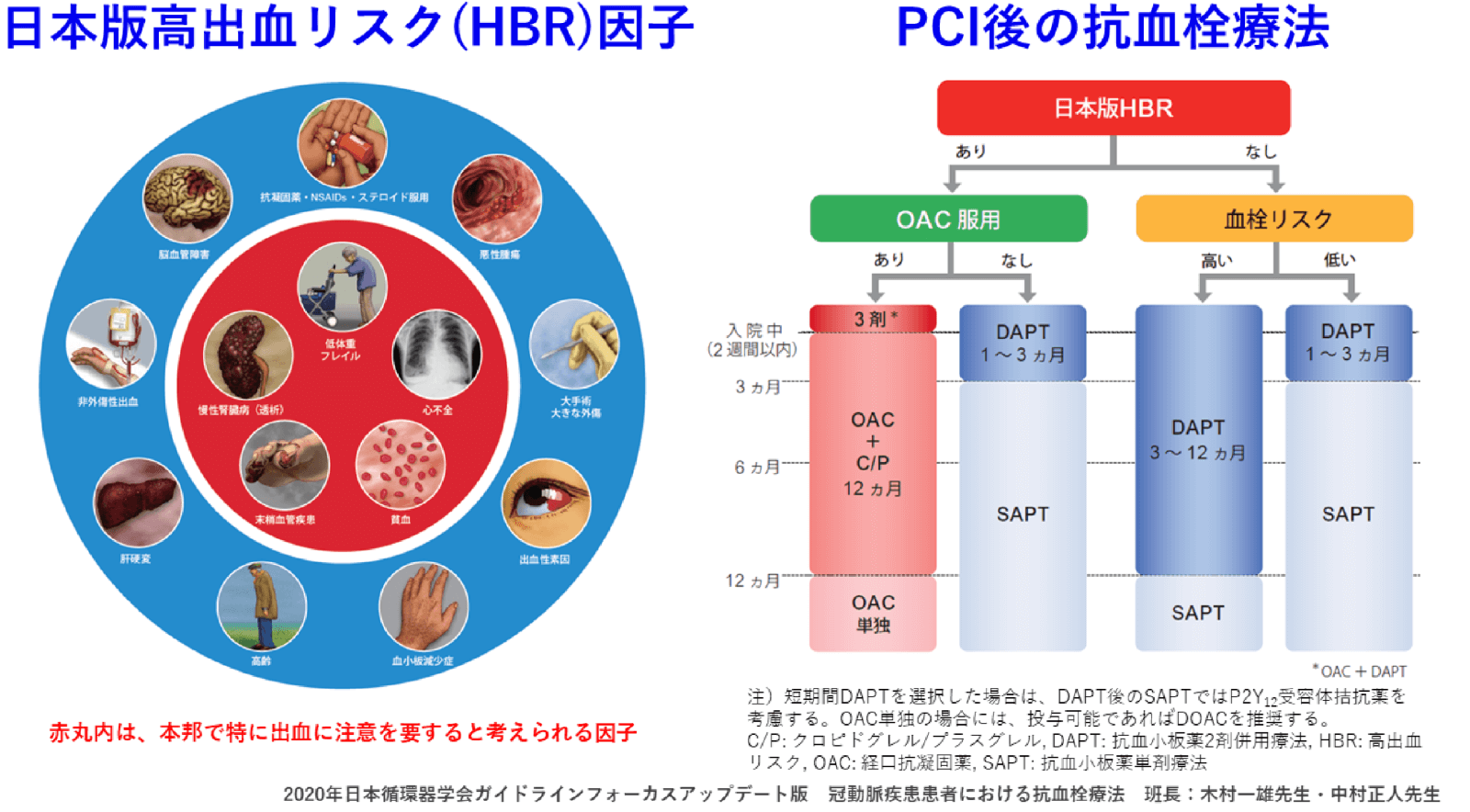
- 高出血リスク(HBR)の患者
1~3ヶ月のDAPT - 非HBRの患者
血栓リスクが低ければ1~3ヶ月、高ければ3~12ヶ月のDAPT - 抗凝固薬服用中の患者
周術期のみ3剤併用、その後1年までは2剤併用、1年以降は抗凝固薬単独
長期治療
DAPTの一定期間後は、抗血小板薬または抗凝固薬の単剤療法を継続します。
高出血リスク(HBR)とPCI後の抗血栓療法の推奨
動脈硬化の進展予防
PCI後の心疾患再発は、治療した病変部位の再狭窄によって生じるよりも、それ以外の部位における冠動脈病変の進行によって起こることの方が多いことが知られています。
動脈硬化の予防
PCI後も動脈硬化の進展を予防することが重要です。そのためには、以下の危険因子を適切に管理することが必要です。
- 高血圧
- 高コレステロール血症
- 糖尿病
- 喫煙
- 肥満
管理方法
危険因子を管理するためには、食事療法、運動療法、禁煙といったライフスタイルの改善に加え、薬物治療が大切になります。特に、コレステロールを下げる治療(脂質低下療法)は重要です。
ガイドラインの推奨
- 日本循環器学会
LDLコレステロール(悪玉コレステロール)を70mg/dL未満にすることを推奨 - ヨーロッパ心臓病学会
LDLコレステロールを55mg/dL未満にすることを推奨
脂質低下療法の薬物治療
スタチンやエゼチミブといった経口薬に加え、皮下注射によるコレステロール低下薬も利用可能です。これらの薬剤を活用した脂質低下療法が、虚血性心疾患の発症・再発予防に有効であるという多くの臨床試験成績が報告されています。
